Sie befinden sich hier
Inhalt
Willkommen im Neurochirurgischen Labor für Neuroonkologie und Tumorbiologie
In unserem Labor widmen wir uns der Erforschung von Glioblastomen, einer der aggressivsten und heterogensten Hirntumorarten. Unser Ziel ist es, die biologischen Mechanismen, die das Tumorwachstum, die interzelluläre Kommunikation und die Resistenz gegenüber bestehenden Therapien antreiben, besser zu verstehen.


Dr. med. Oluwadamilola Akanji, MSc
Facharzt


Cecric Becker
Physik Masterstudent
Kollaborationsprojekt mit der AG Prof. Weidemüller,
Physikalisches Institut, Universität Heidelberg

Julius Beichert
Wissenschaftlicher Mitarbeiter

Julia Maresa Busch
Wissenschaftliche Mitarbeiterin

Jena Kim
Wissenschaftliche Mitarbeiterin

Niklas Zimmermann
Wissenschaftlicher Mitarbeiter
Alumni
Dr. med. Jonathan Bergner
Glioblastomnetzwerke in organotypischen Kulturen
Zusammenfassung:
Glioblastome sind hochaggressive, invasive Tumoren des zentralen Nervensystems, die aufgrund ihrer ausgeprägten Therapieresistenz eine hohe Letalität aufweisen. Diese Resistenzen entstehen unter anderem durch die Interaktion zwischen Tumorzellen und gesundem neuronalem Gewebe sowie durch die Bildung von Tumormikroröhrchen-assoziierten Tumorzellnetzwerken. Da herkömmliche Zellkulturen die Morphologie und das funktionelle Tumorzellnetzwerk nur unzureichend abbilden können und in vivo-Mausmodelle mit erheblichem Aufwand, Kosten und ethischen Bedenken verbunden sind, besteht ein dringender Bedarf an alternativen Modellen für präklinische Therapietestungen.
In dieser Arbeit wurde ein Glioblastommodell auf Basis organotypischer Schnittkulturen etabliert. Hierfür wurden 275 µm dicke Gehirnschnitte juveniler Mäuse in Kultur gehalten und humane Glioblastomzellen implantiert. Nach einer dreiwöchigen Kultivierungsphase erfolgte die Analyse der Tumornetzwerke durch immunfluoreszenzbasierte Färbung. Die resultierenden Tumornetzwerke wurden mit zwei etablierten Modellen verglichen: einer 2D-Monolayerkultur und einem in vivo-Mausmodell. Im Fokus der Analyse standen insbesondere die Länge und Anzahl der gebildeten Tumormikroröhrchen.
Die durchgeführten Analysen zeigten signifikante Unterschiede in der Netzwerkbildung zwischen den drei Gruppen. Während sich die Netzwerke der organotypischen Kulturen deutlich von denen der Monolayerkulturen unterschieden, wiesen sie die größten Abweichungen im Vergleich zum in vivo-Mausmodell auf. Dennoch konnten zentrale glioblastomspezifische morphologische Merkmale in den organotypischen Kulturen nachgewiesen werden.
Obwohl es derzeit noch an standardisierten Gütekriterien für die Eignung von Tumornetzwerken in Therapietests fehlt, zeigen die Ergebnisse, dass organotypische Schnittkulturen ein vielversprechendes Vortestmodell für Tierversuche darstellen können. Diese Kulturen ermöglichen die Abbildung relevanter, glioblastomspezifischer Mechanismen und bieten damit eine wertvolle Plattform für die Testung neuer Therapieansätze. Angesichts der ersten laufenden klinischen Studien, die auf netzwerkspezifische Therapien für Glioblastome abzielen, besteht ein wachsender Bedarf an Modellen, die schnell und reproduzierbar patientenspezifisches Therapieansprechen auf diese innovativen Behandlungsstrategien testen können. Organotypische Schnittkulturen könnten hier eine entscheidende Rolle spielen, indem sie dazu beitragen, den Bedarf an in vivo-Experimenten zu reduzieren und gleichzeitig die Entwicklung zielgerichteterer Therapien zu beschleunigen.
Dr. med. Till Vincent Helm
Einfluss von Musik und Geräuschunterdrückung während Tumorresektionen mit Wachphase auf die subjektiv empfundene und die objektive gemessene Stressbelastung des Patienten
Zusammenfassung:
Die vorliegende Studie wurde an der Neurochirurgischen Klinik der Universitätsmedizin Mannheim, mit dem Ziel durchgeführt, den Patientenkomfort bei Tumorresektionen mit Wachphase zu verbessern. Diese Operationstechnik ist entscheidend für die sichere Entfernung von Tumoren in der Nähe sprachrelevanter Hirnareale. Sie ist jedoch mit einer erhöhten Stressbelastung für die betroffenen Patienten verbunden. Aus diesem Grund wurde in interdisziplinärer Zusammenarbeit ein Audio-Kommunikations-Headset mit geräuschunterdrückenden Kopfhörern entwickelt.
Für die Studie wurden zehn geeignete Patienten rekrutiert, die alle erforderlichen Einschlusskriterien erfüllten. Die Erfassung der subjektiven Stressbelastung erfolgte mittels eines Fragebogens, der eine visuelle Analogskala verwendete. Zur Bestimmung der objektiven Stressbelastung wurden verschiedene Parameter der HRV, der EDA und des EEG analysiert. Die Erfassung der subjektiven und objektiven Stressbelastung erfolgte intraoperativ zu Beginn der Wachphase der Operation während einer Ruhephase sowie im Verlauf der Wachphase während der Musikintervention. Die Auswertung erfolgte sowohl auf intraindividueller als auch auf interindividueller Ebene. Für die retrospektive Analyse der Gesamtdauer der Operationen und der Dauer der Wachphasen wurde eine Kontrollgruppe von zwanzig Patienten herangezogen, die vor der Einführung des Audio-Kommunikations-Headsets in derselben Klinik wach operiert worden waren. Die statistische Auswertung erfolgte mittels Student’s t-Test und des Mann-Whitney-U-Test.
Alle Patienten berichteten, dass sie die Musik während der Operation als beruhigend und angenehm empfanden. Der Fragebogen zeigte, dass drei von acht Patienten eine allgemeine Stressreduktion durch die Musik erlebten. Während der Musikintervention zeigte die HRV-Analyse eine durchschnittliche Verlängerung der RR-Intervalle um ca. 10% (p < 0,001). Gleichzeitig wurde eine signifikante Reduktion des LF/HF-Verhältnisses beobachtet (p = 0,014). Andere HRV-Parameter wie SDNN und rMSSD zeigten einen signifikanten Anstieg während der Musikintervention. Die EDA zeigte eine mittlere Reduktion der unspezifischen Hautleitfähigkeitsreaktionen während der Musikintervention. Sowohl die Auswertung der EDA als auch die des EEG lieferten jedoch aufgrund technischer Probleme keine eindeutig verwertbaren Ergebnisse. Der retrospektive Vergleich der Gesamtdauer der Operationen ergab keine Unterschiede in der Dauer. Allerdings war die Wachphase in der Gruppe, die mit dem Audio-Kommunikations-Headset operiert wurde, um 22,6% kürzer als in der Kontrollgruppe (45 ± 27,3 Minuten vs. 61,8 ± 22,9 Minuten; p = 0,049).
Die Ergebnisse dieser Studie legen nahe, dass der Einsatz des hier vorgestellten Audio-Kommunikations-Headsets in Kombination mit Musik die intraoperative Stressbelastung der Patienten während einer Tumorresektion mit Wachphase reduzieren kann. Darüber hinaus könnte dies zu einer signifikanten Verkürzung der Dauer der Wachphase während solcher Operationen führen.
Steffen Schlieper-Scherf
Disrupting glioblastoma networks with tumor treating fields (TTFields) in in vitro models
Abstract:
Purpose: This study investigates the biological effect of Tumor Treating Fields (TTFields) on key drivers of glioblastoma's malignancy-tumor microtube (TM) formation-and on the function and overall integrity of the tumor cell network.
Method: Using a two-dimensional monoculture GB cell network model (2DTM) of primary glioblastoma cell (GBC) cultures (S24, BG5 or T269), we evaluated the effects of TTFields on cell density, interconnectivity and structural integrity of the tumor network. We also analyzed calcium (Ca2+) transient dynamics and network morphology, validating findings in patient-derived tumoroids and brain tumor organoids.
Results: In the 2DTM assay, TTFields reduced cell density by 85-88% and disrupted network interconnectivity, particularly in cells with multiple TMs. A "crooked TM" phenotype emerged in 5-6% of treated cells, rarely seen in controls. Ca2+ transients were significantly compromised, with global Ca2+ activity reduced by 51-83%, active and periodic cells by over 50%, and intercellular co-activity by 52% in S24, and almost completely in BG5 GBCs. The effects were more pronounced at 200 kHz compared to a 50 kHz TTFields. Similar reductions in Ca2+ activity were observed in patient-derived tumoroids. In brain tumor organoids, TTFields significantly reduced tumor cell proliferation and infiltration.
Conclusion: Our comprehensive study provides new insights into the multiple effects of Inovitro-modeled TTFields on glioma progression, morphology and network dynamics in vitro. Future in vivo studies to verify our in vitro findings may provide the basis for a deeper understanding and optimization of TTFields as a therapeutic modality in the treatment of GB.
Keywords: Cancer cell network; Cancer neuroscience; Glioma; TTFields; Tumor microtubes.
Anika Simon PhD
Unsere Forschungsschwerpunkte
Tumorzellnetzwerke und Interzelluläre Kommunikation
Wir analysieren, wie Glioblastomzellen durch spezialisierte Strukturen, sogenannte Tumormikrotubes, miteinander verbunden sind. Diese Netzwerke ermöglichen nicht nur die Kommunikation zwischen Zellen, sondern tragen auch zur Invasion, Proliferation und Therapieresistenz bei.

Präklinische Modelle zur Untersuchung von Therapien
Unser Labor nutzt innovative präklinische Modelle, darunter patientenabgeleitete Tumoroide und Hirntumororganoide, um die Wirkung von Medikamenten und externen Einflüssen von verschiedenen Medikamenten oder von elektrischen Feldern auf Tumorzellnetzwerke zu untersuchen.

Heterogenität und Neuro-Krebs-Interaktionen
Wir erforschen, wie glioblastomassoziierte Zellen zwischen verschiedenen Zuständen wechseln, darunter invasive, einzeln agierende Zellen und dicht vernetzte Zellcluster. Dabei untersuchen wir auch, wie neuronale und krebsbedingte Mechanismen zur Krankheitsprogression beitragen.
Unser Labor widmet sich dem besseren Verständnis der Glioblastom-Heterogenität sowie der Entwicklung, präklinischen Testung und Abbildung neuer Therapieansätze. Dafür sind vielseitige Tumormodelle und Primärzelllinien unverzichtbar. Als Teil von UNITE Glioblastoma („Understanding and Targeting Resistance in Glioblastoma“) arbeiten wir eng mit Ärzt:innen und Wissenschaftler:innen des Universitätsklinikums Heidelberg, des Universitätsklinikums Mannheim, des Deutschen Krebsforschungszentrums und der Hochschule Mannheim zusammen, um innovative Lösungen für die Behandlung dieser komplexen Tumorerkrankung zu entwickeln.
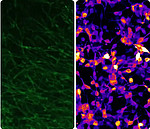
Movie: Calcium Signaling in GBC Monolayers and Brain Organoids Infiltrated With Tumor Cells
Live-Aufnahmen von GCaMP8s-markierten Kalziumoszillationen in einem 2D-Kulturmodell menschlicher Glioblastomzellen sowie in einem Glioblastom-Spheroid, das innerhalb eines Gehirnorganoids wächst. Die verwendeten Organoide stammen aus der Arbeitsgruppe von Haiku Liu (https://www.dkfz.de/molekulare-neurogenetik) und wurden mit Tumorzellen injiziert, um die Interaktion von Tumor- und Hirngewebe zu untersuchen.
Die dynamischen Veränderungen der Kalziumkonzentration verdeutlichen die aktive Ionenregulation innerhalb des Zellverbundes. Diese Prozesse spielen eine zentrale Rolle in der Kommunikation und Funktion des Tumorzellnetzwerks.
Unser Ansatz
Mit modernsten Technologien wie 2D- und 3D-Livezellmikroskopie sowie genetisch kodierten Reportersystemen (z. B. Kalziumreportern) erfassen wir dynamische Prozesse in Echtzeit. Diese Daten helfen uns, ein detailliertes Verständnis für die strukturelle und funktionelle Integrität von Tumorzellnetzwerken zu entwickeln und potenzielle Schwachstellen für therapeutische Eingriffe zu identifizieren.
Unsere Vision
Unser Ziel ist es, die molekularen, zellulären und funktionellen Unterschiede von Glioblastomen besser zu verstehen, um Therapieansätze gezielt zu untersuchen und weiterzuentwickeln.